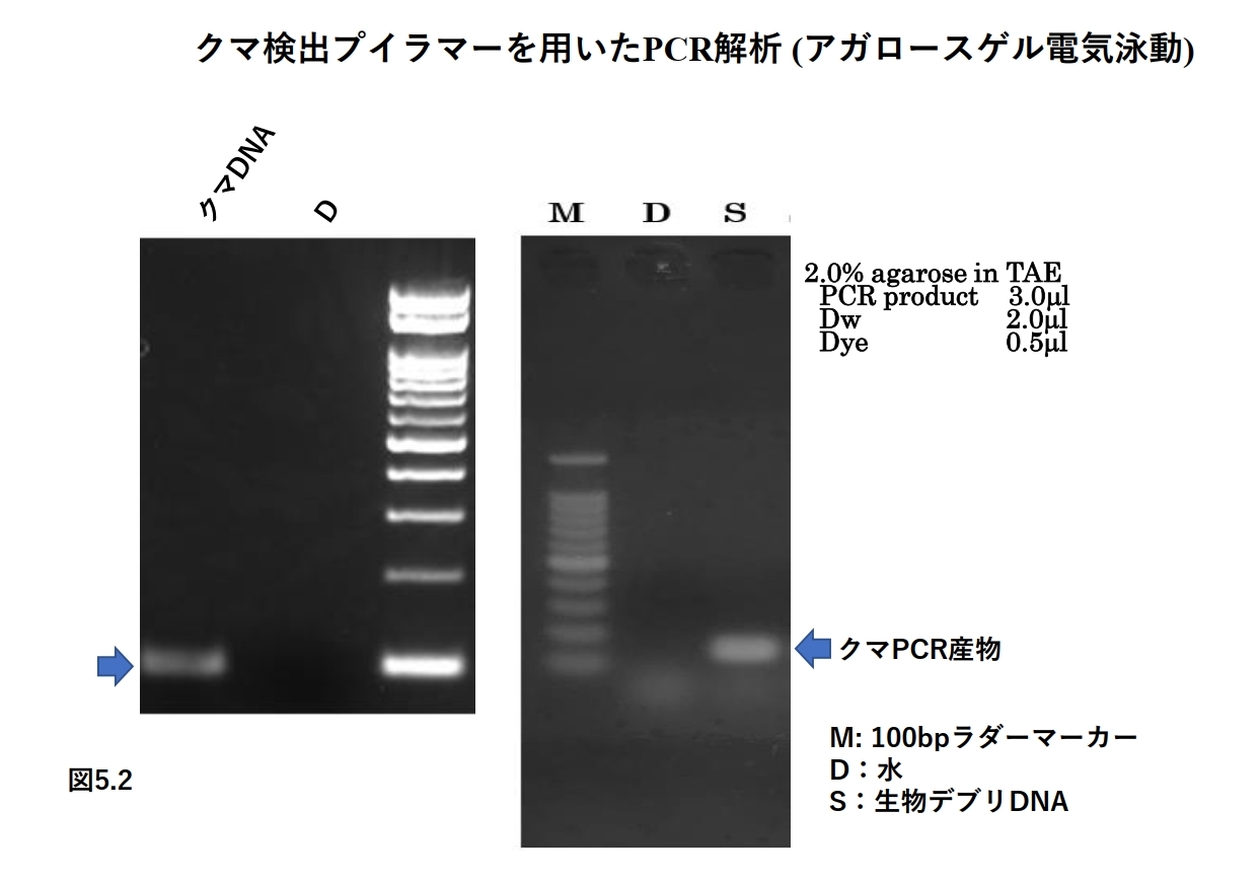
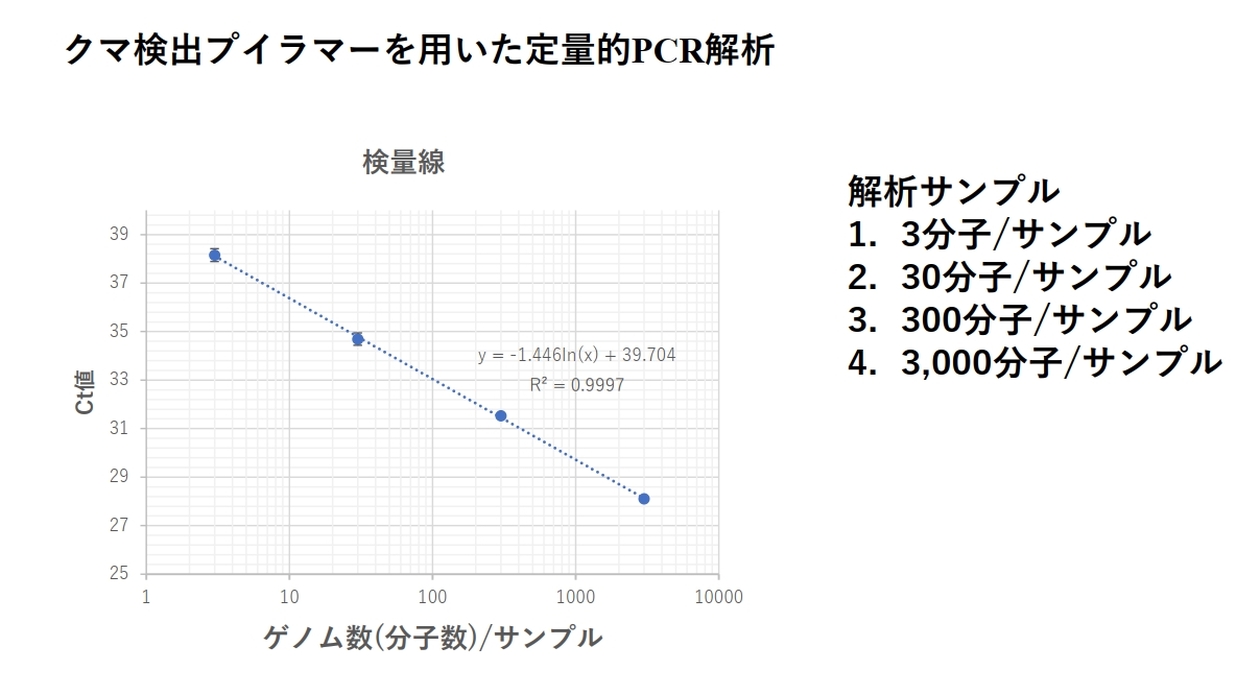
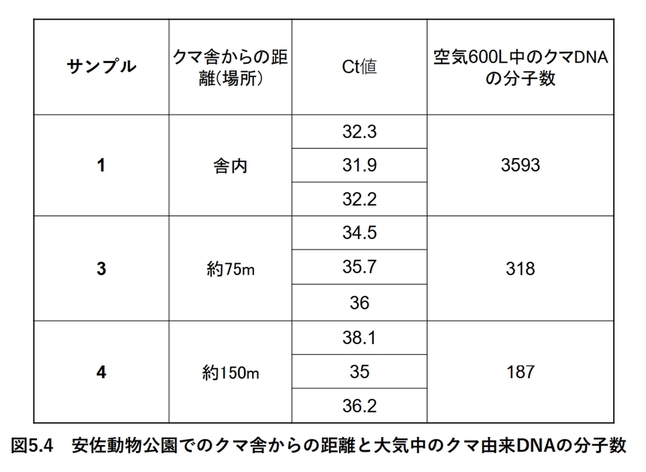
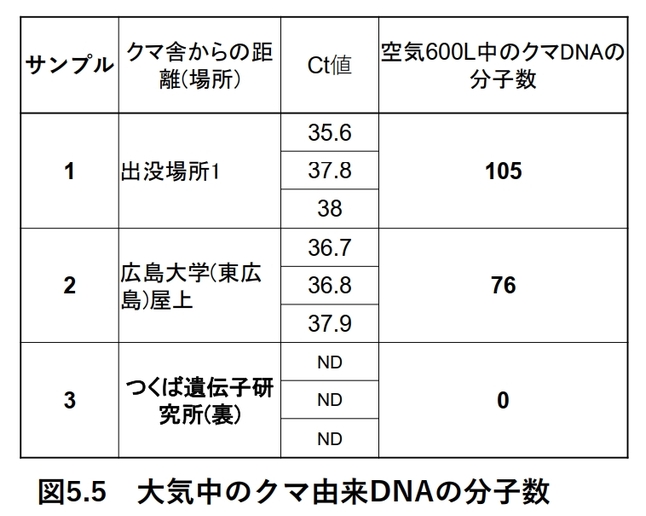
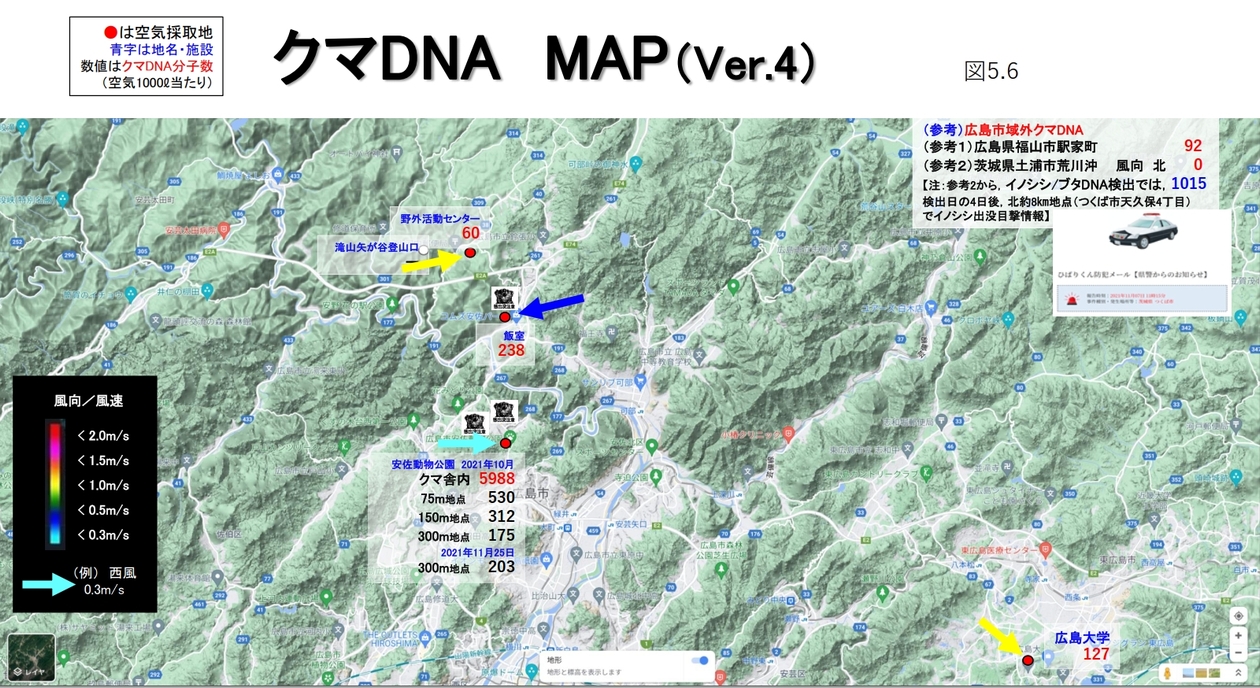
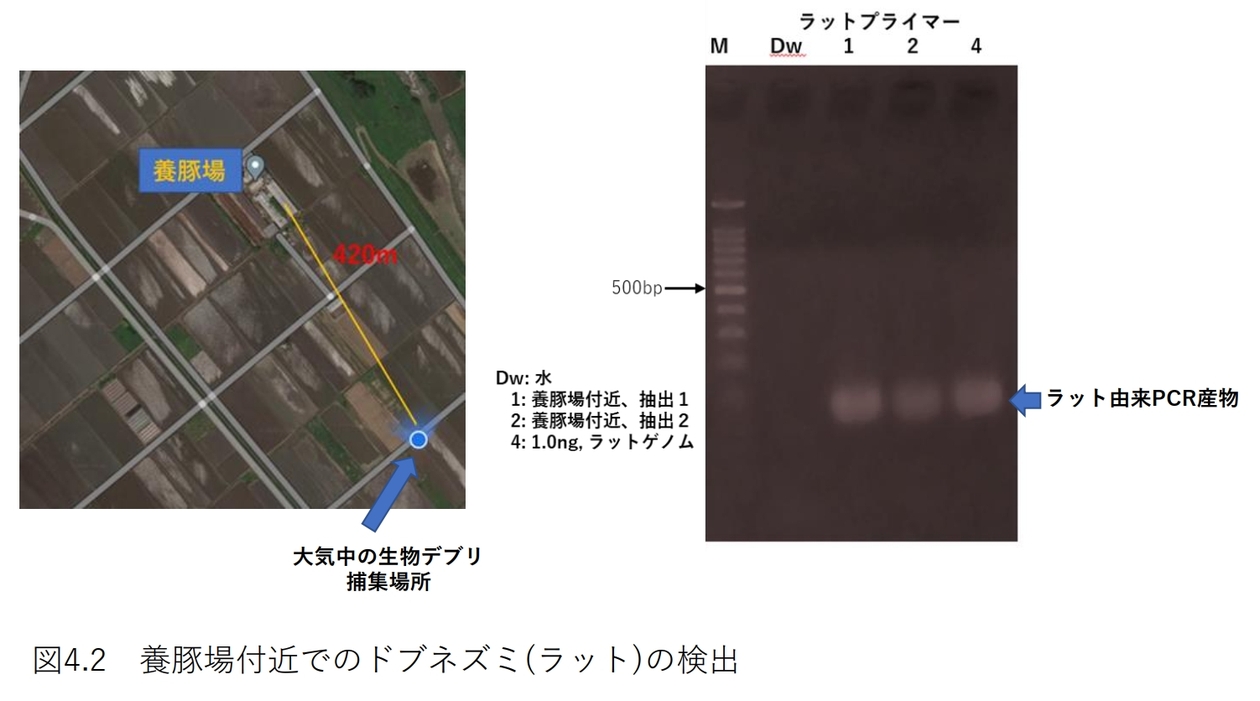
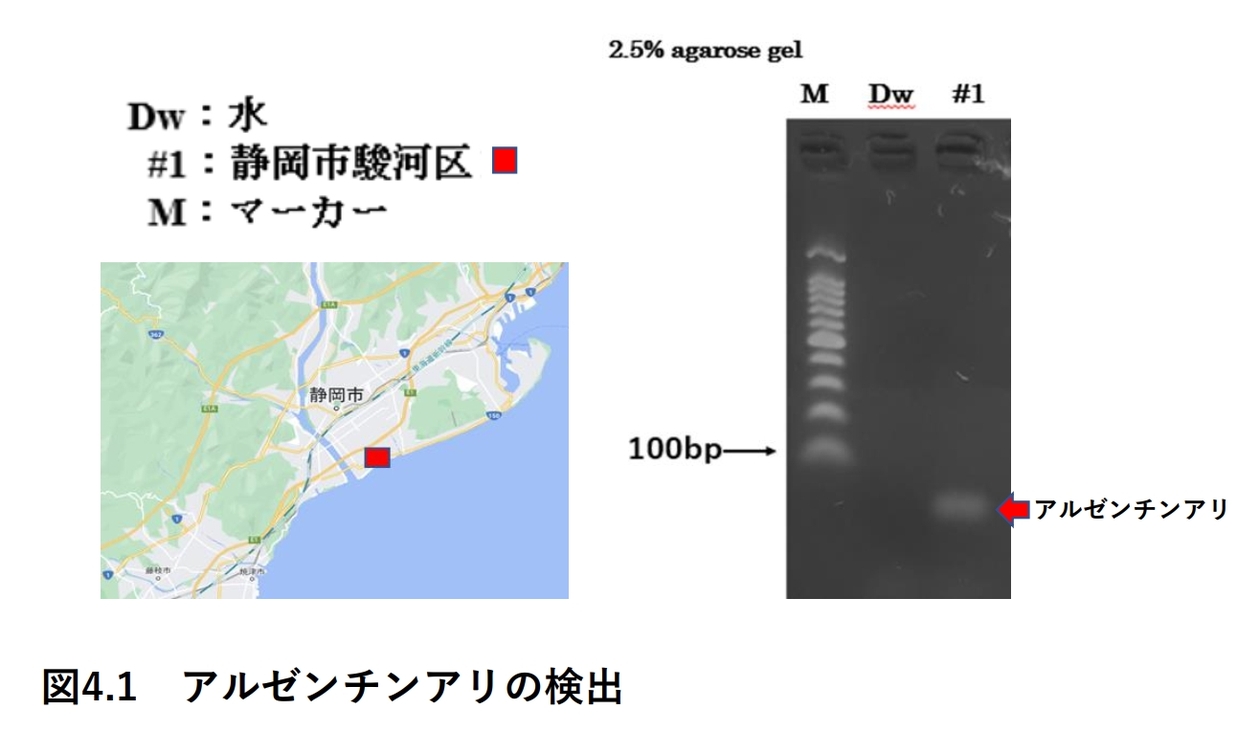
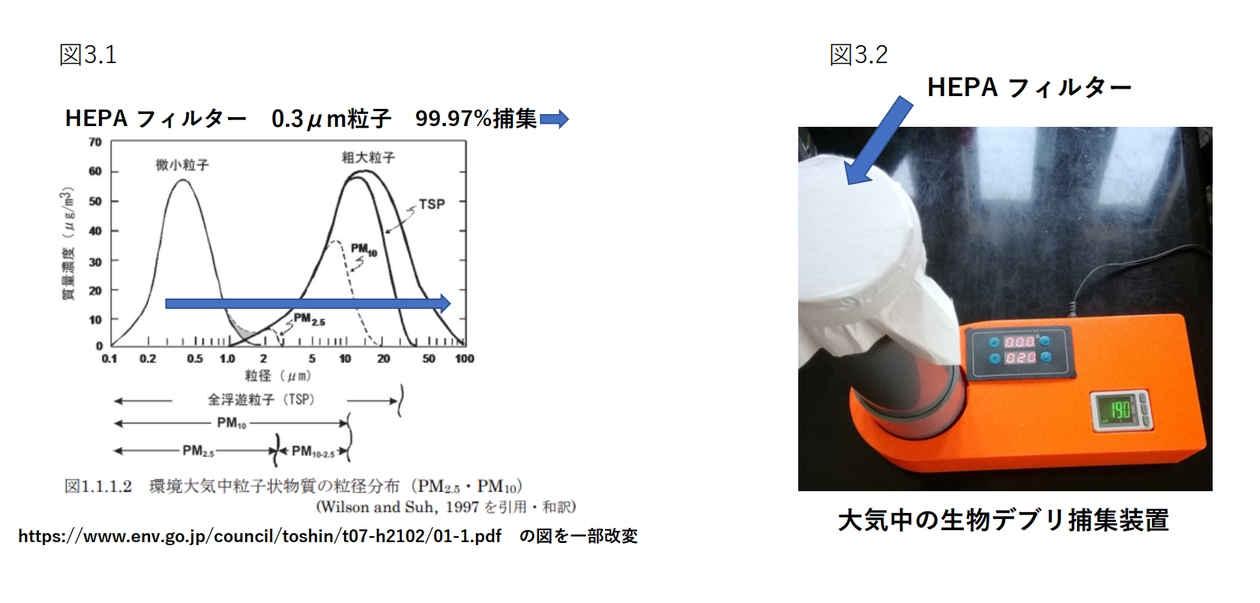
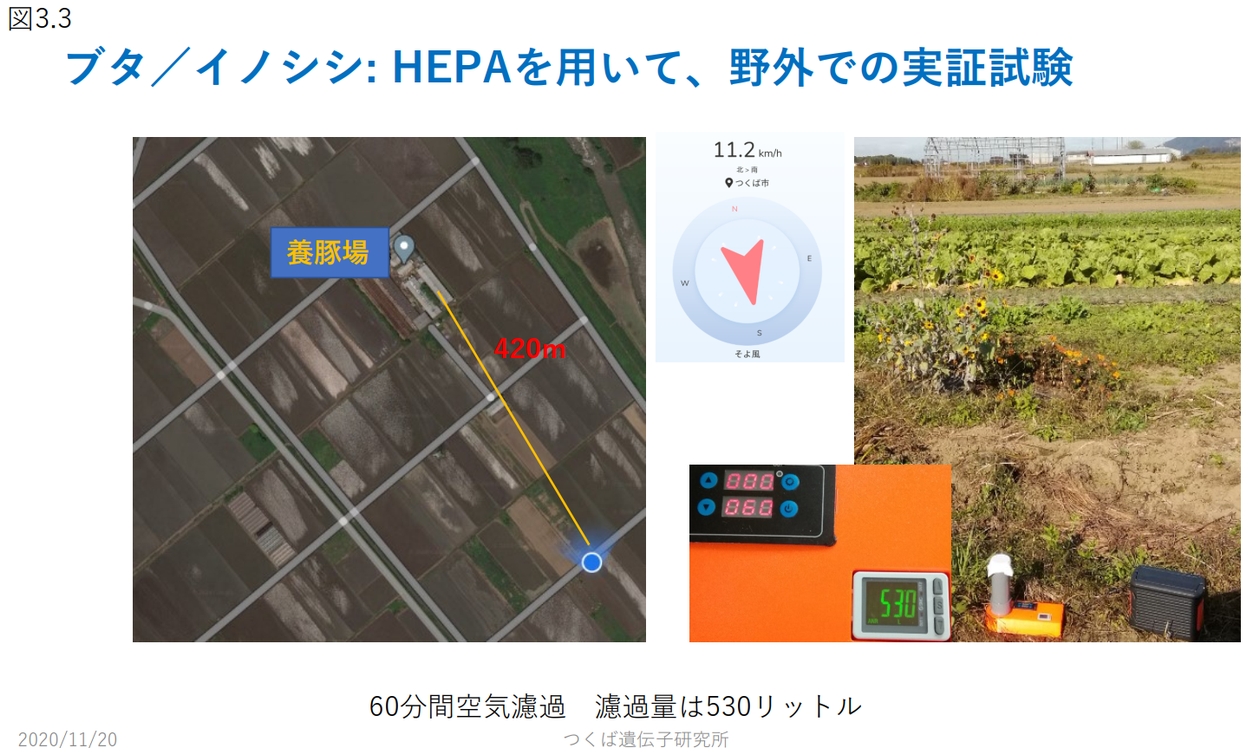
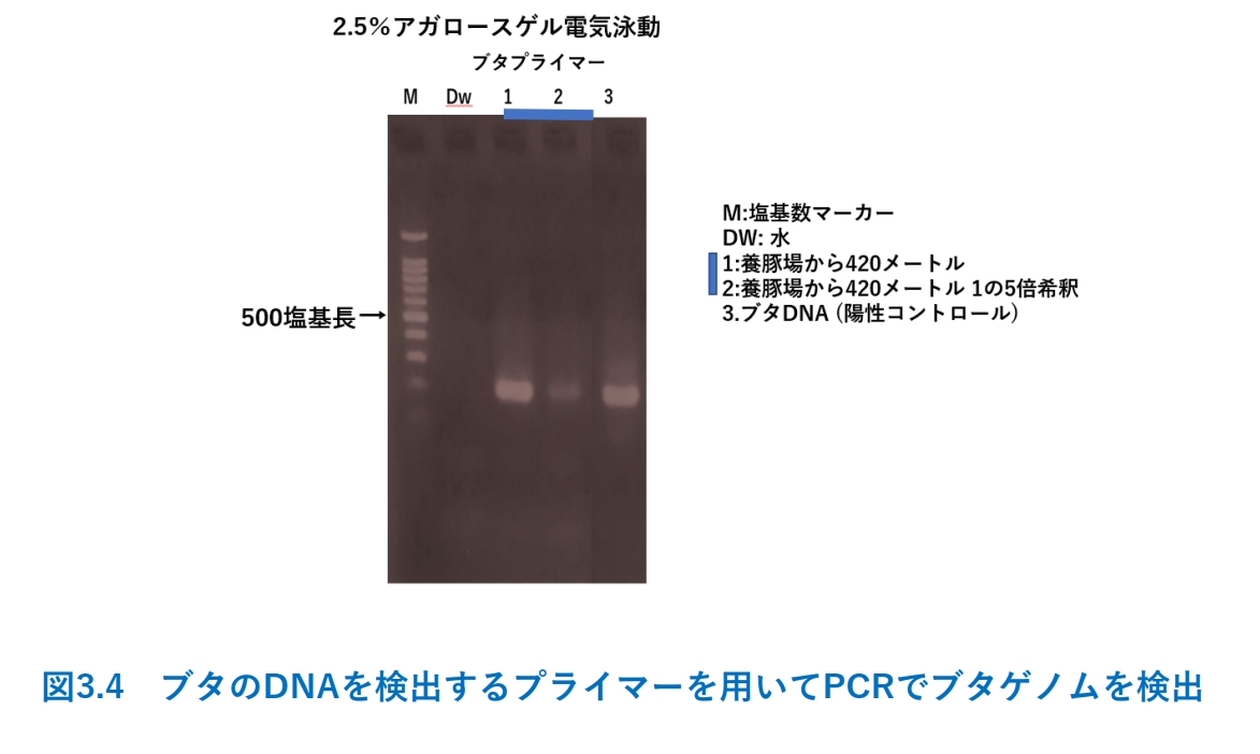
これまで、クマなど、哺乳類由来の大気中の生物デブリについて述べてきました。そして、クマのデブリの解析では、空気中のデブリの量を数値化できるようにしたこともお伝えしました。この結果を応用して、空気中の病害微生物の量も捕捉可能ではないかと考えました。そこで、今、問題となっている鳥インフルエンザについて考察してみたいと思います。
◆鳥インフルエンザウィルスの捕捉
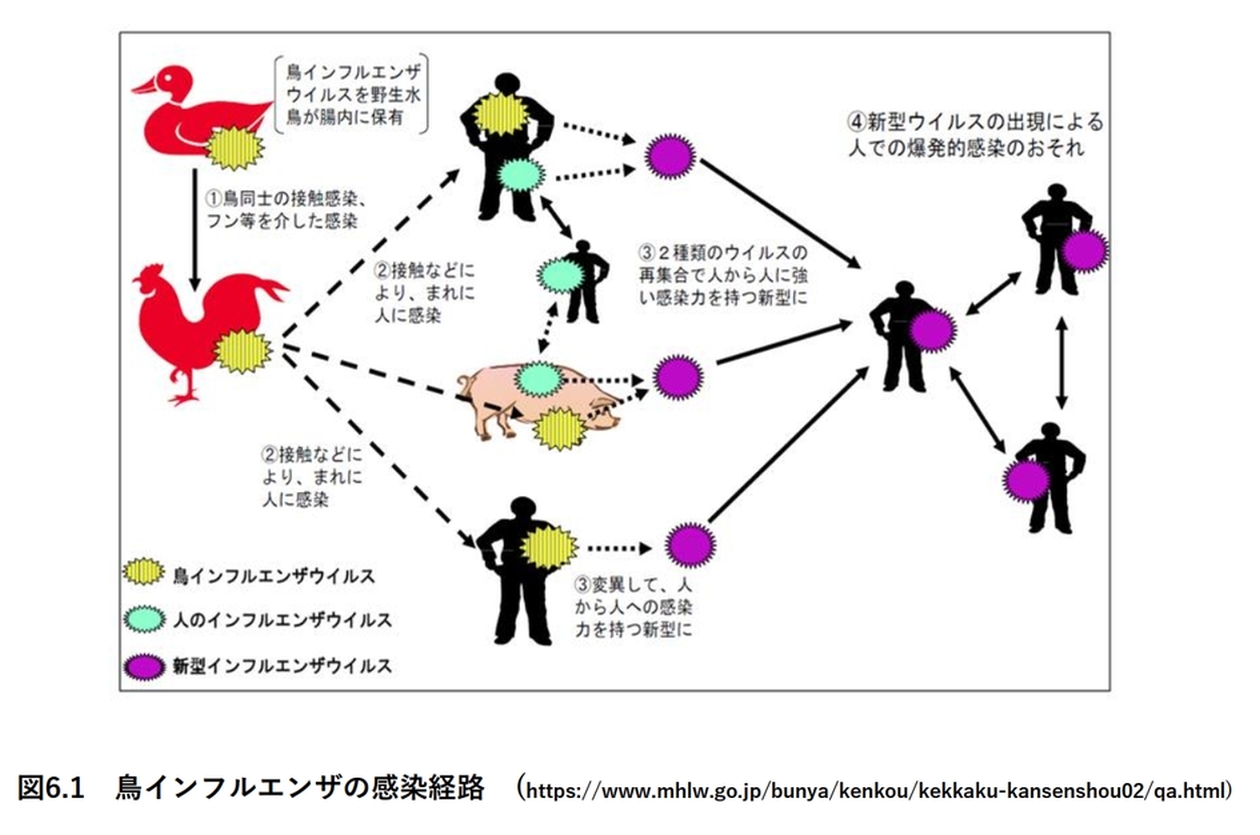
鳥インフルエンザは、現在、我が国のみならず世界の鶏舎で猛威を振るっています。鳥インフルエンザは、鳥インフルエンザウィルスによって引き起こされる鳥の感染症です。農林水産省のサイト(サイト1)に、「鳥インフルエンザは、A型インフルエンザウイルスが引き起こす鳥の病気です。鳥に感染するA型インフルエンザウイルスをまとめて鳥インフルエンザウイルスといいます。これを、家畜伝染病予防法では、家きん(ニワトリ、七面鳥等)に対する病原性やウイルスの型によって、「高病原性鳥インフルエンザ」、「低病原性鳥インフルエンザ」などに分類しています。家きんで高病原性鳥インフルエンザが発生すると、その多くが死んでしまいます。一方、低病原性鳥インフルエンザの発生では、「症状が出ない場合もあれば、咳や粗い呼吸などの軽い呼吸器症状が出たり産卵率が下がったりする場合もあります。」と記載されています。そのため、鳥インフルエンザが発生した養鶏場では、感染拡大を阻止するため、そこで飼育されているニワトリすべてを殺処分します。2022/23年シーズンは、10月末に岡山県倉敷市、北海道厚真町で確認されて以降、23県で57事例が発生。1シーズンの殺処分数としては過去最多だった2020年度の987万羽を超え、1月10日時点で1008万羽となっています(サイト2)。
その結果、物価の優等生と言われてきた鶏卵も価格高止まり状態が続いており、我々の家計には大きな負担となっています。
そのうえ、1997年香港において、当時、生きた鳥を売買している市場で流行していた高病原性の鳥インフルエンザA(H5N1)ウイルスが、ヒトに伝播し感染者が18人確認され、そのうち6人が死亡した (サイト3)例があり、今年2023年にもカンボジアで少女が死亡、その父親も感染しました。
このように、人間に対する病原性にも注意が必要です[図6.1]。
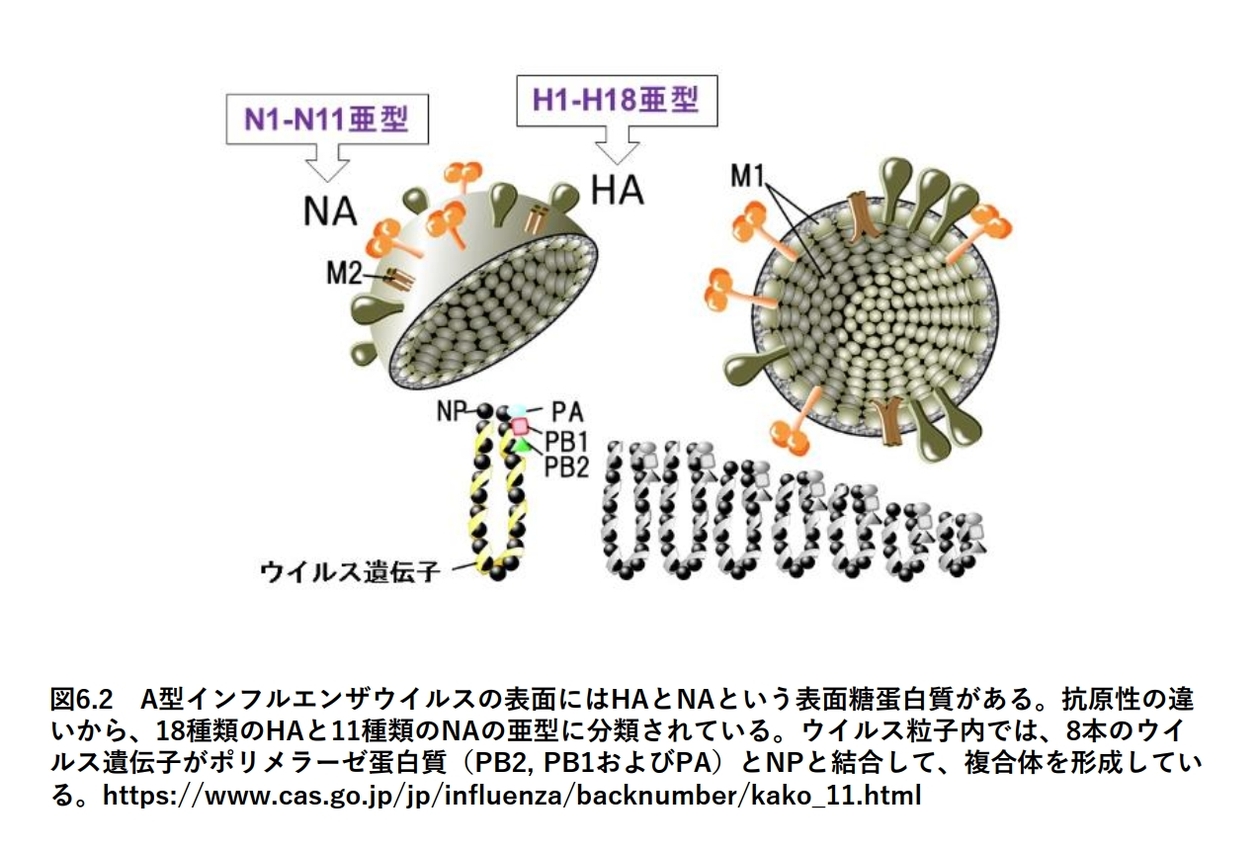
インフルエンザウイルスはエンベロープ(外套膜)(直径80-120nm)に覆われた球形のウイルスで、粒子内部には直接メッセンジャーRNA(mRNA)とはならない8 分節したRNA、及びA、B、Cの型を担う核タンパク(NP)、並びに膜タンパク(M1)などを持っています[図6.2](サイト3)。RNAは、8個の分節からなっており、その全体の長さは約13キロ塩基です(サイト4)。感染経路は、感染した渡り鳥の糞、体液が大気中に拡散し、浮遊物となって、鶏舎等に侵入し、鶏舎内のニワトリに感染が広がると思われます。
もし、我々が使っている大気中の生物デブリ捕集システムを使って、ウイルスの存在・量を解析すると仮定したなら、先ず、集めた大気中の生物デブリからRNAを抽出します。この場合、抽出したRNAをすぐに鋳型として解析することはできないので、コロナウイルスの場合と同様に、一旦RNAリバーストランスクリプテースと呼ばれる酵素を用いて、DNAに変換しその後、PCR法で解析することになります。以前は2ステップ法、つまり試験管操作が二回必要でしたが、2006年に一回の試験管操作で、ウイルスRNAをDNAに変換し、そのままPCRを進めて、その解析結果の取得まで行える方法が開発されました。
これにより、サンプル以外のRNA、DNA(例えば操作をするヒト由来とか)などの混入 (コンタミネーション)が起こる可能性も低く抑えることが出来ました。この時同時に、この解析に必要なプイラマーセットも作製されました(論文1)。
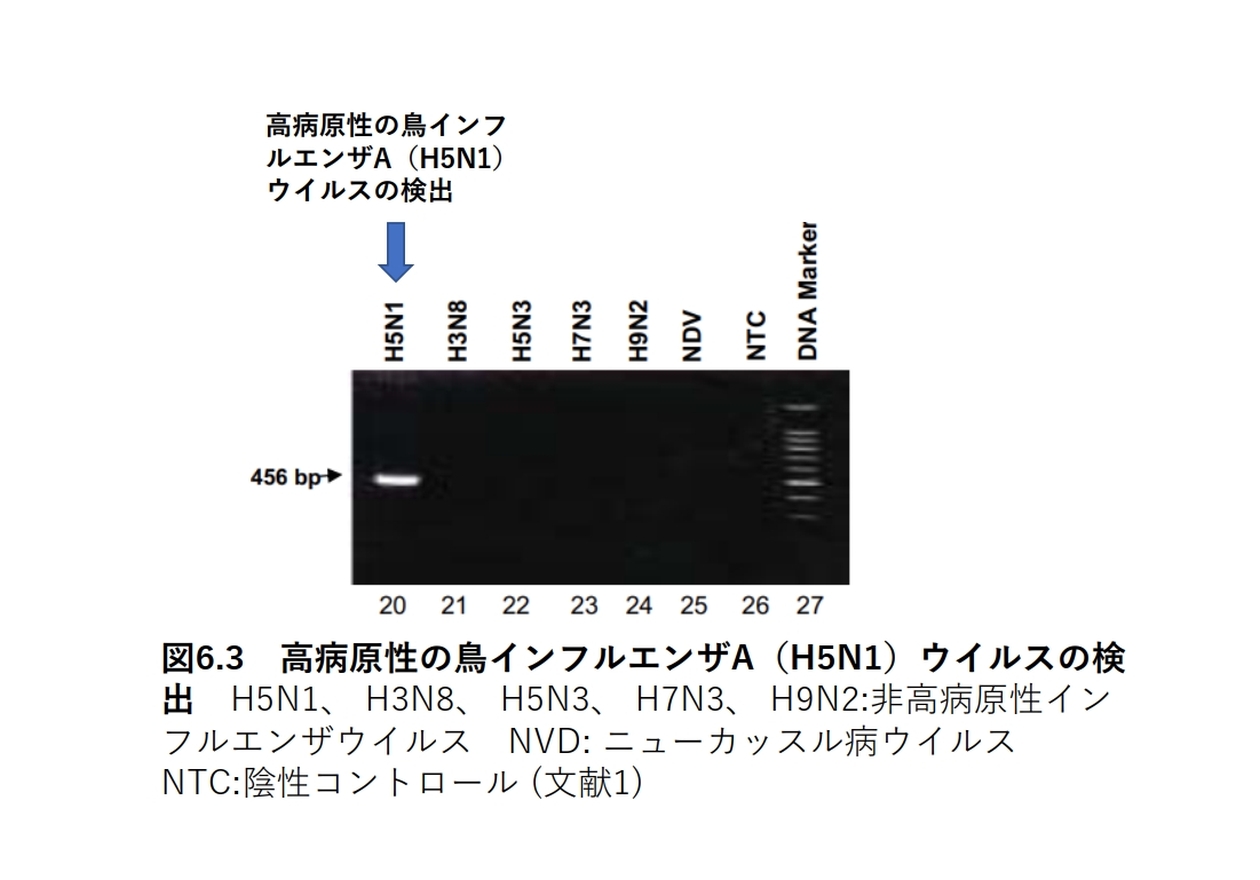
ワンステップ逆転写 (RT)-PCR システム と 高病原性の鳥インフルエンザA(H5N1)ウイルス特異的プライマー (フォワードプライマー:5′-ACTATGAAGAATTGAAACACCT-3′ および逆プライマー:5′-GCAATGAAATTTCCATTACTCTC-3’)を用いて解析する方法です。この方法では、高病原性の鳥インフルエンザA(H5N1)ウイルスが特異的に検出されています[図6.3]。
現在、我々は、実際に解析したデータは持ち合わせていませんが、近い将来、捕集した大気中の生物デブリを用いて、高病原性の鳥インフルエンザA(H5N1)ウイルスの検出にトライしてみる予定です。トライした結果が出ましたら、改めてご報告したいと思います。
野外からの鳥インフルエンザウィルス感染阻止の対策として、現在私が考える方法は、コロナウイルス感染防止で医療者が使用しているマスクのN95フィルター、或いはさらに、目の細かい、我々が生物デブリの捕集に使用しているHEPAフィルターを使って、鶏舎に入る外気をろ過して清浄化し、かつ、出入りや隙間を防ぐ目的で鶏舎内を陽圧に保つことです。しかし、それにかかる費用は高いと思われ、畜産農業生産に見合うかどうかは難しいところです。
サイト1 https://www.maff.go.jp/j/syouan/douei/tori/know.html
サイト2 https://www.nippon.com/ja/japan-data/h01560/
サイト3 https://www.cas.go.jp/jp/influenza/backnumber/kako_11.html
サイト4 https://www.ncbi.nlm.nih.gov/data-hub/taxonomy/11320/
論文1 Specific detection of H5N1 avian influenza A virus in field specimens by a one-step RT-PCR assay. Lisa FP Ng, Ian Barr, Tung Nguyen, Suriani Mohd Noor, Rosemary Sok-Pin Tan, Lora V Agathe, Sanjay Gupta, Hassuzana Khalil, Thanh Long To, Sharifah Syed Hassan and Ee-Chee Ren. BMC Infectious Diseases2006, 6:40
◎安江 博 わかりやすい!科学の最前線
〈01〉生き物の根幹にある核酸
〈02〉ヒトのゲノム解析分析の進歩
〈03〉DNAがもたらす光と影[1]
〈04〉DNAがもたらす光と影[2]
〈05〉生物種の生存圏
〈06〉大気中の生物デブリ捕集装置を用いたアルゼンチンアリの生存圏の解析 静岡市にはまだアルゼンチンアリが生息していた!
〈07〉大気中の生物デブリ捕集装置を用いた、ドブネズミ(ラット属)の生存圏の解析 この環境にドブネズミはいるのか、いないのか?
〈08〉大気中の生物デブリ捕集装置を用いた、クマ(クマ科)の生存圏の解析
〈09〉大気中の生物デブリ捕集装置を用いた病害微生物の検出
▼安江 博(やすえ・ひろし)
1949年、大阪生まれ。大阪大学理学研究科博士課程修了(理学博士)。農林水産省・厚生労働省に技官として勤務、愛知県がんセンター主任研究員、農業生物資源研究所、成育医療センターへ出向。フランス(パリINRA)米国(ミネソタ州立大)駐在。筑波大学(農林学系)助教授、同大学(医療系一消化器外科)非常勤講師等を経て、現在(株)つくば遺伝子研究所所長。著書に『一流の前立腺がん患者になれ! 最適な治療を受けるために』(鹿砦社)等
◎鹿砦社 http://www.rokusaisha.com/kikan.php?group=ichi&bookid=000686
四六判/カバー装 本文128ページ/オールカラー/定価1,650円(税込)